
试验信息
试验分期:Ⅰ期、Ⅱ期、Ⅲ期
药品名称:SHR-A1811
适应症:经治复发/转移宫颈癌、卵巢癌、子宫内膜癌
患者画像:HER2 表达的妇科恶性肿瘤患者(包括复发性卵巢癌、子宫内膜癌、宫颈癌患者)
试验专业题目
评价注射用SHR-A1811治疗HER2表达晚期宫颈癌、复发性卵巢癌及子宫内膜癌的有效性、安全性。
主要入选标准
1、18~75 周岁,ECOG 评分:0~1 分,预期生存期≥12 周;
2、研究分别入组晚期宫颈癌、复发性卵巢癌及子宫内膜癌患者:
队列 1 复发性卵巢癌:
组织病理学确诊的复发性卵巢上皮癌、输卵管癌或原发性腹膜癌,既往经过以铂类为基础的方案治疗,且最后一次含铂治疗方案治疗期间或治疗结束(完成 4 程及以上治疗)后<6 个月进展或复发;针对铂耐药/铂难治复发性卵巢癌,接受过不超过 1 个非铂方案治疗。
注:复发或进展的定义(满足以下任一条件):a)有明确记录的影像学进展;b)CA-125 持续升高。
队列 2 子宫内膜癌:
组织病理学确诊的子宫内膜癌(除外癌肉瘤),经过初始治疗后出现复发/转移的患者;既往针对复发/转移阶段经过至少 1 线、且不超过 2 线系统治疗(除外放疗增敏的化疗),治疗期间或治疗结束后出现疾病复发或进展。
队列 3 宫颈癌:
组织或细胞学证实的宫颈癌;既往针对复发/转移性宫颈癌经过至少 1 线、且不超过 2 线系统治疗(除外放疗增敏的化疗),治疗期间或治疗结束后出现疾病复发或进展;
注:新辅助或辅助治疗(除外放疗增敏的化疗),如在初始治疗规范手术后 1 年、放疗后 6个月内疾病复发、进展,计为一线系统治疗。
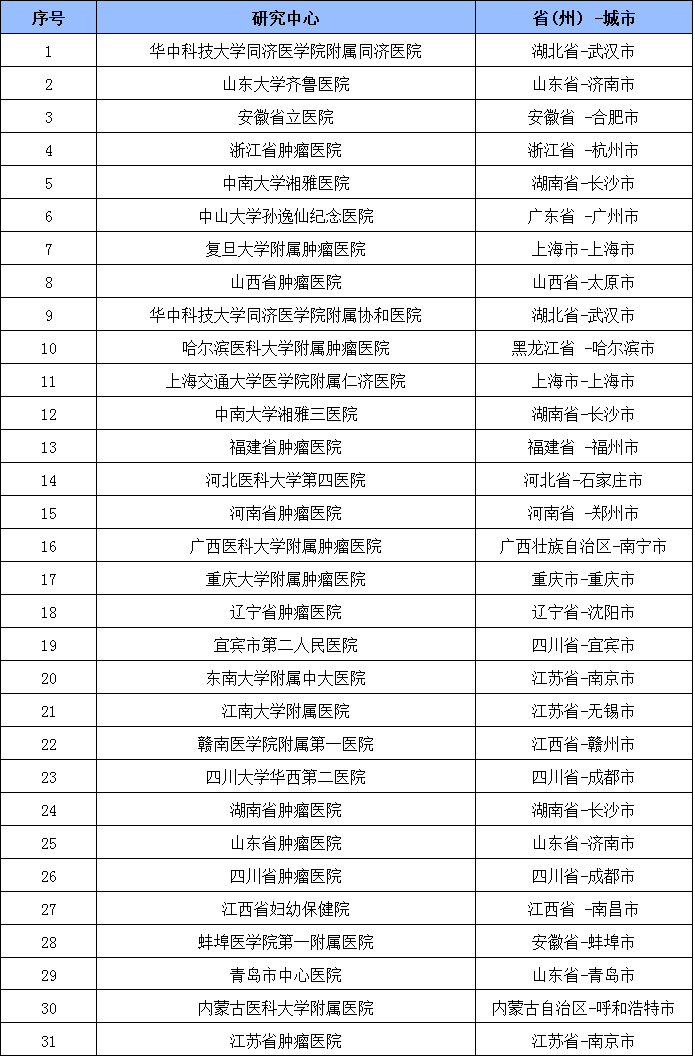
参与机构
试验信息
试验分期:Ⅰ期、Ⅱ期、Ⅲ期
药品名称:SHR-A1811
适应症:经治复发/转移宫颈癌、卵巢癌、子宫内膜癌
患者画像:HER2 表达的妇科恶性肿瘤患者(包括复发性卵巢癌、子宫内膜癌、宫颈癌患者)
试验专业题目
评价注射用SHR-A1811治疗HER2表达晚期宫颈癌、复发性卵巢癌及子宫内膜癌的有效性、安全性。
主要入选标准
1、18~75 周岁,ECOG 评分:0~1 分,预期生存期≥12 周;
2、研究分别入组晚期宫颈癌、复发性卵巢癌及子宫内膜癌患者:
队列 1 复发性卵巢癌:
组织病理学确诊的复发性卵巢上皮癌、输卵管癌或原发性腹膜癌,既往经过以铂类为基础的方案治疗,且最后一次含铂治疗方案治疗期间或治疗结束(完成 4 程及以上治疗)后<6 个月进展或复发;针对铂耐药/铂难治复发性卵巢癌,接受过不超过 1 个非铂方案治疗。
注:复发或进展的定义(满足以下任一条件):a)有明确记录的影像学进展;b)CA-125 持续升高。
队列 2 子宫内膜癌:
组织病理学确诊的子宫内膜癌(除外癌肉瘤),经过初始治疗后出现复发/转移的患者;既往针对复发/转移阶段经过至少 1 线、且不超过 2 线系统治疗(除外放疗增敏的化疗),治疗期间或治疗结束后出现疾病复发或进展。
队列 3 宫颈癌:
组织或细胞学证实的宫颈癌;既往针对复发/转移性宫颈癌经过至少 1 线、且不超过 2 线系统治疗(除外放疗增敏的化疗),治疗期间或治疗结束后出现疾病复发或进展;
注:新辅助或辅助治疗(除外放疗增敏的化疗),如在初始治疗规范手术后 1 年、放疗后 6个月内疾病复发、进展,计为一线系统治疗。
参与机构
