
试验分期:Ⅲ期
药品名称:QX005N注射液
适应症:中度至重度特应性皮炎(AD)
患者画像:12~70 岁,IGA 评分≥3;EASI 评分≥16;AD 受累面积 BSA≥10%;每日 PP-NRS 评分的周平均值≥4 分(18岁成人患病时间≥1年,≥12岁且<18岁青少年患病时间≥6个月)的特应性皮炎患者。
主要入选标准
1) 筛选时,12~70岁(含界值),性别不限。注:年龄<18岁青少年受试者体重需≥30 kg;
2) 筛选时诊断为特应性皮炎(根据美国皮肤病学会一致性标准,2014),且在筛选和基线时,根据研究者评估,AD受累程度同时符合以下标准:
a) 筛选时≥18岁成人患病时间≥1年,≥12岁且<18岁青少年患病时间≥6个月;
b) IGA评分≥3;EASI评分≥16;AD受累面积BSA≥10%;每日PP-NRS评分的周平均值≥4分(7天中,要求至少要有4天的评分用于基线平均分计算。如果原计划随机化日期前7天中,受试者的报告天数低于4天,应推迟随机化,直至符合要求,但不得超出筛选的最长期限28天);
c) 经研究者判断:受试者对中至超强效皮质类固醇(TCS)等外用药物疗效不佳或不适宜进行外用药物治疗(如有重要的副作用或安全性风险,如严重的局部感染、皮肤萎缩、毛细血管扩张等)。注:疗效不佳定义为:1、在基线前的1年中连续使用中强效TCS治疗≥28天或超强效TCS≥14天,但仍未实现并维持缓解,并且也未达到低疾病活动状态(相当于IGA 0=无症状至2=轻度)。2、接受过规范的AD系统治疗;
主要排除标准
1)随机前12个月内,酒精(定义为每天饮酒>2单位/每周饮酒>14单位,饮酒1单位相当360 mL啤酒或45 mL酒精含量40%的烈酒或150 mL葡萄酒)或药物滥用者;
2)曾接受以下任何一种治疗:
a) 既往接受过抗白介素-4 受体α(IL-4Rα)或白介素-13(IL- 13)抗体治疗;
b) 随机前2周内使用过用于治疗AD或有可能影响AD病情评估的外用药物,包括但不限于TCS、外用钙调磷酸酶抑制剂(TCI)、外用磷酸二酯酶-4(PDE-4)抑制剂、外用Janus激酶(JAK)抑制剂、芳香烃受体激动剂,或外用的含有中药成分的一类药物(包括中药方剂、草药、中成药等)(注:用于治疗AD之外的其他疾病,根据研究者和/或专科医生的医学判断,认为确有必要使用,也不会干扰研究评估的情况除外)等;
c) 随机前2周内使用过处方润肤剂或含有添加剂(如神经酰胺、透明质酸、尿素,或者丝聚蛋白分解产物)或含有止痒成分(如薄荷醇、多羟基乙醇、普拉莫辛、利多卡因、普利洛卡因、辣椒素、纳曲酮、N-棕榈酰乙醇胺等)的润肤剂(研究统一提供的基础润肤剂除外);
d) 随机前1周使用抗组胺药物(在随即前已经稳定使用抗组胺药物持续治疗至少7天,且计划在研究期间持续使用的可以入组);
e) 随机前2周内使用过以复方甘草酸苷、白芍总苷等为主要活性成分的药物(如复方甘草酸苷片);
f) 随机前4周内进行过漂白浴;
g) 随机前4周内因AD或其他疾病接受过皮质类固醇或其他免疫抑制/免疫调节药物(如环孢素、霉酚酸酯、硫唑嘌呤、甲氨蝶呤、口服JAK抑制剂或口服PDE-4抑制剂等)的全身治疗(皮质类固醇吸入剂和鼻喷剂除外);
h) 随机前12个月内接受过任何细胞耗竭疗法(包括但不限于抗CD20、抗CD52、抗CD4、抗CD5、抗CD3、抗CD19疗法);
i) 随机前3个月内或5个药物半衰期内(如果已知)使用其他免疫调节类生物制剂,以时间较长者为准;
j) 随机前4周内使用口服或系统性的含有AD治疗作用的中药成分的药物(包括中药方剂、草药、中成药等)(注:用于治疗AD之外的其他疾病,根据研究者和/或专科医生的医学判断,认为确有必要使用,也不会干扰研究评估的情况除外);
k) 随机前4周内接受光疗(窄谱紫外线B[NB-UVB]、宽谱紫外线 B[BB-UVB] 、 紫外线A1[UVA1] 、补骨脂素+ 紫外线 A[PUVA])、日晒床或任何其他发光装置(LED)治疗;
l) 随机前3个月或至少5个半衰期(以时间较长者为准)内参加过其他药物临床试验,或随机前3个月内参加过医疗器械临床试验;
m) 随机前3个月内接种过任何活疫苗、减毒活疫苗,或计划在研究期间接种活疫苗、减毒活疫苗;
n) 随机前6个月内接受变应原特异性免疫疗法(SIT)治疗(筛选前已处于稳定剂量且继续在试验期间保持稳定的受试者除外)。
3) 筛选和基线时存在可能干扰研究评估的其他皮肤疾病或症状表现。
4) 筛选前6个月内存在活动性春季角膜结膜炎(VKC)和特应性角膜结膜炎(AKC)病史。
5) 筛选时研究者判定有严重的疾病史且经研究者判断不适宜进入研究,包括但不限于不稳定的心脏(如II-III度房室传导阻滞、心功能评估为纽约心脏病协会[NYHA]III/IV级等严重的心脏疾病)、肺、肾脏、消化系统疾病等。
6) 筛选时有恶性肿瘤病史者(已成功治疗且生存5年以上无复发证据的皮肤鳞状细胞癌、基底细胞癌、宫颈原位癌除外)。
7) 筛选时可能存在活动性结核感染情况,或既往有结核病史。
8) 筛选时有乙型肝炎或丙型肝炎或梅毒筛查阳性或有人类免疫缺陷病毒(HIV)感染。
9) 筛选时存在以下任何一项实验室检查异常:
➢ 天冬氨酸转氨酶或丙氨酸转氨酶(AST/ALT)>1.5 倍正常值上限,或总胆红素(TBIL)>1.5 倍正常值上限;
➢血清肌酐(SCr)>1.5 倍正常值上限;
➢ 其他实验室检查结果异常,经研究者判断可能影响受试者完成试验或干扰试验结果。
注:如受试者筛选时存在以上实验室检查结果异常,经研究者评估认为必要,可允许在筛选期 28 天内的不同日安排 1 次复查,复查后合格可允许入组(复查前不允许对异常实验室检查结果进行药物干预)。
10) 筛选前2周内因较严重的感染需院内就诊并规律使用相应的全身性抗感染治疗,或随机前1周内因病情轻微的感染类疾病(如上呼吸道感染等)需使用抗感染类药物或患有可能干扰研究评估的浅表皮肤感染(感染消退后,由研究者根据受试者的情况判断是否可以入组)。
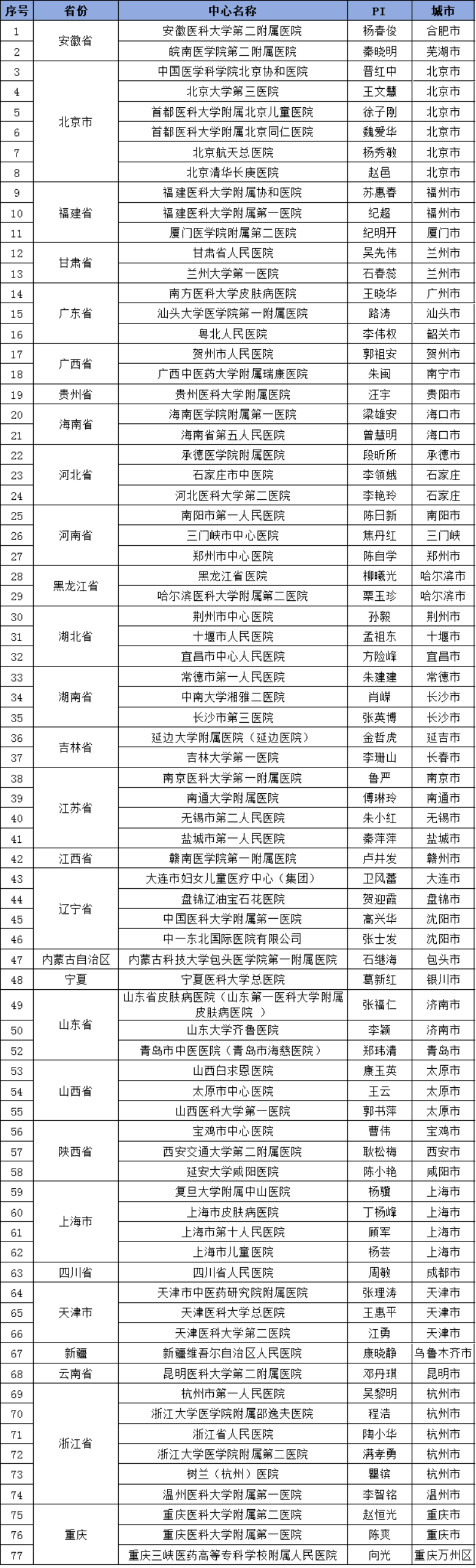
研究中心
试验分期:Ⅲ期
药品名称:QX005N注射液
适应症:中度至重度特应性皮炎(AD)
患者画像:12~70 岁,IGA 评分≥3;EASI 评分≥16;AD 受累面积 BSA≥10%;每日 PP-NRS 评分的周平均值≥4 分(18岁成人患病时间≥1年,≥12岁且<18岁青少年患病时间≥6个月)的特应性皮炎患者。
主要入选标准
1) 筛选时,12~70岁(含界值),性别不限。注:年龄<18岁青少年受试者体重需≥30 kg;
2) 筛选时诊断为特应性皮炎(根据美国皮肤病学会一致性标准,2014),且在筛选和基线时,根据研究者评估,AD受累程度同时符合以下标准:
a) 筛选时≥18岁成人患病时间≥1年,≥12岁且<18岁青少年患病时间≥6个月;
b) IGA评分≥3;EASI评分≥16;AD受累面积BSA≥10%;每日PP-NRS评分的周平均值≥4分(7天中,要求至少要有4天的评分用于基线平均分计算。如果原计划随机化日期前7天中,受试者的报告天数低于4天,应推迟随机化,直至符合要求,但不得超出筛选的最长期限28天);
c) 经研究者判断:受试者对中至超强效皮质类固醇(TCS)等外用药物疗效不佳或不适宜进行外用药物治疗(如有重要的副作用或安全性风险,如严重的局部感染、皮肤萎缩、毛细血管扩张等)。注:疗效不佳定义为:1、在基线前的1年中连续使用中强效TCS治疗≥28天或超强效TCS≥14天,但仍未实现并维持缓解,并且也未达到低疾病活动状态(相当于IGA 0=无症状至2=轻度)。2、接受过规范的AD系统治疗;
主要排除标准
1)随机前12个月内,酒精(定义为每天饮酒>2单位/每周饮酒>14单位,饮酒1单位相当360 mL啤酒或45 mL酒精含量40%的烈酒或150 mL葡萄酒)或药物滥用者;
2)曾接受以下任何一种治疗:
a) 既往接受过抗白介素-4 受体α(IL-4Rα)或白介素-13(IL- 13)抗体治疗;
b) 随机前2周内使用过用于治疗AD或有可能影响AD病情评估的外用药物,包括但不限于TCS、外用钙调磷酸酶抑制剂(TCI)、外用磷酸二酯酶-4(PDE-4)抑制剂、外用Janus激酶(JAK)抑制剂、芳香烃受体激动剂,或外用的含有中药成分的一类药物(包括中药方剂、草药、中成药等)(注:用于治疗AD之外的其他疾病,根据研究者和/或专科医生的医学判断,认为确有必要使用,也不会干扰研究评估的情况除外)等;
c) 随机前2周内使用过处方润肤剂或含有添加剂(如神经酰胺、透明质酸、尿素,或者丝聚蛋白分解产物)或含有止痒成分(如薄荷醇、多羟基乙醇、普拉莫辛、利多卡因、普利洛卡因、辣椒素、纳曲酮、N-棕榈酰乙醇胺等)的润肤剂(研究统一提供的基础润肤剂除外);
d) 随机前1周使用抗组胺药物(在随即前已经稳定使用抗组胺药物持续治疗至少7天,且计划在研究期间持续使用的可以入组);
e) 随机前2周内使用过以复方甘草酸苷、白芍总苷等为主要活性成分的药物(如复方甘草酸苷片);
f) 随机前4周内进行过漂白浴;
g) 随机前4周内因AD或其他疾病接受过皮质类固醇或其他免疫抑制/免疫调节药物(如环孢素、霉酚酸酯、硫唑嘌呤、甲氨蝶呤、口服JAK抑制剂或口服PDE-4抑制剂等)的全身治疗(皮质类固醇吸入剂和鼻喷剂除外);
h) 随机前12个月内接受过任何细胞耗竭疗法(包括但不限于抗CD20、抗CD52、抗CD4、抗CD5、抗CD3、抗CD19疗法);
i) 随机前3个月内或5个药物半衰期内(如果已知)使用其他免疫调节类生物制剂,以时间较长者为准;
j) 随机前4周内使用口服或系统性的含有AD治疗作用的中药成分的药物(包括中药方剂、草药、中成药等)(注:用于治疗AD之外的其他疾病,根据研究者和/或专科医生的医学判断,认为确有必要使用,也不会干扰研究评估的情况除外);
k) 随机前4周内接受光疗(窄谱紫外线B[NB-UVB]、宽谱紫外线 B[BB-UVB] 、 紫外线A1[UVA1] 、补骨脂素+ 紫外线 A[PUVA])、日晒床或任何其他发光装置(LED)治疗;
l) 随机前3个月或至少5个半衰期(以时间较长者为准)内参加过其他药物临床试验,或随机前3个月内参加过医疗器械临床试验;
m) 随机前3个月内接种过任何活疫苗、减毒活疫苗,或计划在研究期间接种活疫苗、减毒活疫苗;
n) 随机前6个月内接受变应原特异性免疫疗法(SIT)治疗(筛选前已处于稳定剂量且继续在试验期间保持稳定的受试者除外)。
3) 筛选和基线时存在可能干扰研究评估的其他皮肤疾病或症状表现。
4) 筛选前6个月内存在活动性春季角膜结膜炎(VKC)和特应性角膜结膜炎(AKC)病史。
5) 筛选时研究者判定有严重的疾病史且经研究者判断不适宜进入研究,包括但不限于不稳定的心脏(如II-III度房室传导阻滞、心功能评估为纽约心脏病协会[NYHA]III/IV级等严重的心脏疾病)、肺、肾脏、消化系统疾病等。
6) 筛选时有恶性肿瘤病史者(已成功治疗且生存5年以上无复发证据的皮肤鳞状细胞癌、基底细胞癌、宫颈原位癌除外)。
7) 筛选时可能存在活动性结核感染情况,或既往有结核病史。
8) 筛选时有乙型肝炎或丙型肝炎或梅毒筛查阳性或有人类免疫缺陷病毒(HIV)感染。
9) 筛选时存在以下任何一项实验室检查异常:
➢ 天冬氨酸转氨酶或丙氨酸转氨酶(AST/ALT)>1.5 倍正常值上限,或总胆红素(TBIL)>1.5 倍正常值上限;
➢血清肌酐(SCr)>1.5 倍正常值上限;
➢ 其他实验室检查结果异常,经研究者判断可能影响受试者完成试验或干扰试验结果。
注:如受试者筛选时存在以上实验室检查结果异常,经研究者评估认为必要,可允许在筛选期 28 天内的不同日安排 1 次复查,复查后合格可允许入组(复查前不允许对异常实验室检查结果进行药物干预)。
10) 筛选前2周内因较严重的感染需院内就诊并规律使用相应的全身性抗感染治疗,或随机前1周内因病情轻微的感染类疾病(如上呼吸道感染等)需使用抗感染类药物或患有可能干扰研究评估的浅表皮肤感染(感染消退后,由研究者根据受试者的情况判断是否可以入组)。
研究中心
